帝京大学生化学講座は、「難病を治す研究」を生化学と分子生物学の手法からアプローチしています。現在は主に、老化、がん、内分泌代謝疾患の病態の解明、新規診断法及び治療法の開発を目指しています。

M. Adachi
以下、当研究室の研究の概要をご紹介します。興味をお持ちの大学院生、基礎研究医、研究室配属の学部生を歓迎いたします。
老化に関する研究
個体老化をはじめとした加齢性疾患には、細胞老化によって生じる生理活性因子の分泌を示す細胞の蓄積が密接に関わっていることが近年の研究で判明しつつあります。私たちの最新の研究では、内分泌組織として様々なホルモン分泌の役割を担う副腎組織への老化細胞の蓄積が、恒常性を制御するホルモン産生系を撹乱させ、個体老化に結びつくことが分かってきました。つまり、副腎組織のホルモン分泌とその受容体を有する全身の組織における分子ネットワークを解明することが、個体老化を理解するうえで重要であると考えられます。そこで、加齢マウスを使用した動物実験や遺伝子組換え技術を用いることで、副腎を標的にしたマウスや安定細胞株を作製することで、生体内の老化メカニズムを分子レベルで解明し、加齢性疾患に対する新規診断法や治療薬の開発を目指します。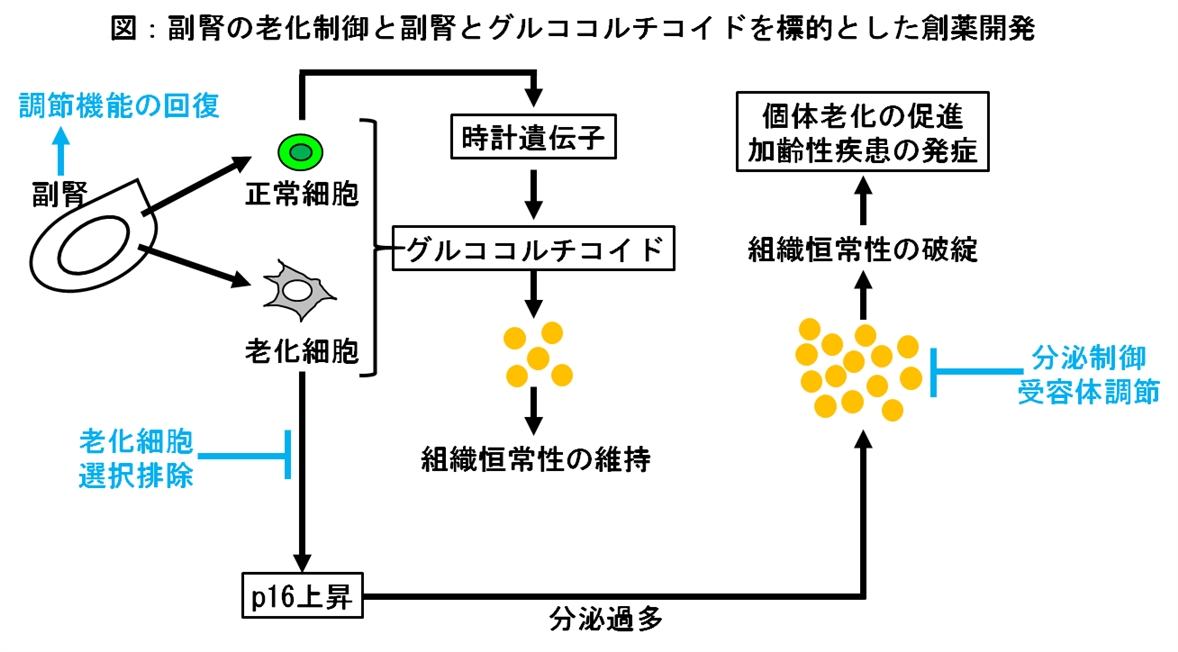

N. Okudaira
現在、「内分泌組織の老化を発端とした個体老化の理解と革新的な抗老化作用薬の探索」というテーマで研究を行っています。
内分泌代謝疾患に関する研究
前立腺がんで抗増殖作用を規定する新規ビタミンD標的遺伝子の探索
生体内では様々な内分泌物質が分泌されることで生体の恒常性が維持され、またこの破綻は様々な内分泌代謝疾患の原因となります。なかでも脂溶性ホルモンと核内受容体は、生体の様々な生理応答を仲介する重要な遺伝子発現制御系です。この厳密な制御軸の破綻は、しばしば発がんや悪性化に寄与し、また新規制御軸の同定は新たな生理機能調節の発見に繋がると期待できます。私たちは、性ステロイドホルモンに応答して増殖する乳がんや前立腺がん主な標的として、脂溶性ホルモン-核内受容体による新規クロストーク機序の探索や抗がん増殖作用を仲介する遺伝子の探索を行っています。現在、アンドロゲン依存的に増殖する前立腺がんで抗増殖作用を示す活性型ビタミンDに着目し、その標的遺伝子群からアンドロゲンシグナリングを阻害する因子の探索を試みています。将来的に難治性がんにも有効な新規治療法の開発を目指します。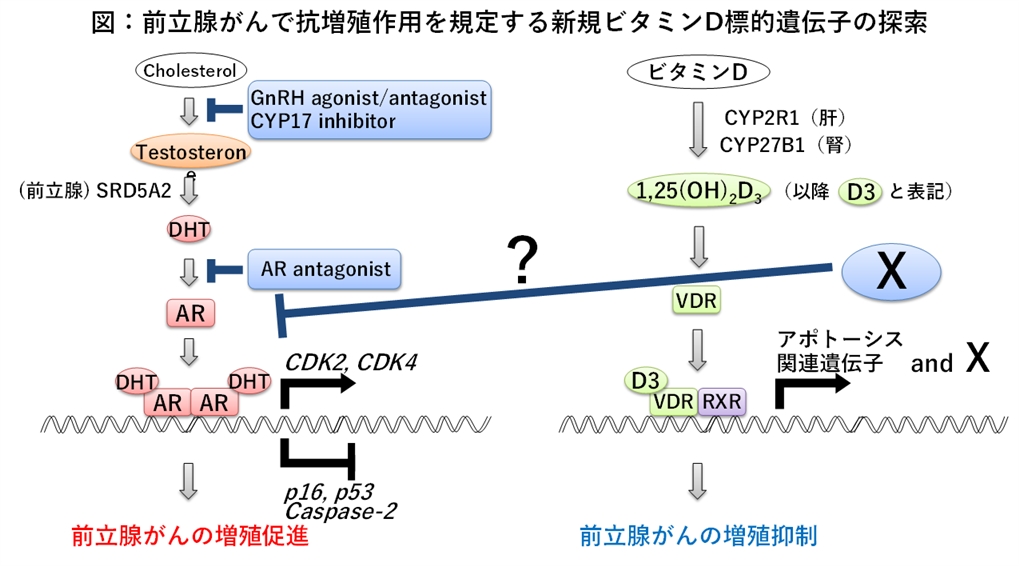

T. Susa
現在、「ゲノム編集を利用したDNAメチル化制御による新規前立腺癌治療戦略の開発」というテーマで研究を行っています。
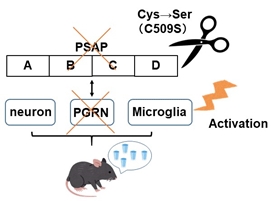
原発性多飲症を発症するサポシンD(SAP-D)欠損マウスの病態解析
- プロサポシン(SAP-A,B,C,Dの前駆体)のDドメインを変異させて作成した本マウスは、口渇中枢(SFO)周辺に炎症を伴う異常をきたし、多飲→多尿→腎障害→多飲の末、腎不全で死亡することを報告した。
- この病態の発症には、プログラニュリン(PGRN)と活性型ミクログリアが関与していることを発見した。
- 現在さらなる解析を進めている。

H. Hisaki
現在、「原発性多飲症を発症するサポシンD(SAP-D)欠損マウスの病態解析」を行っているのは私です。
がんに関する研究
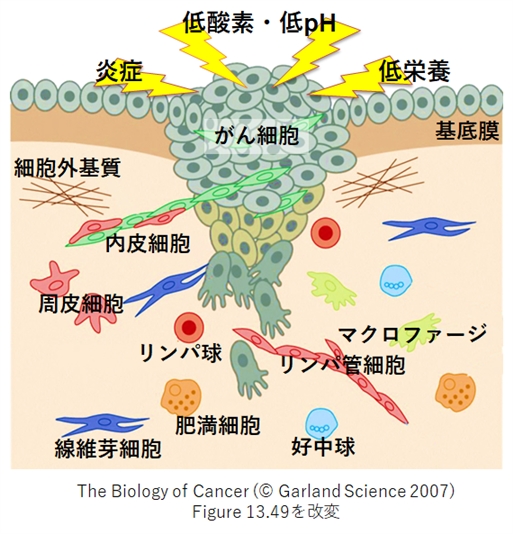
固形がんの腫瘍組織中には、がん細胞以外にも様々な細胞(がん間質細胞)や細胞外基質が混在して相互作用すると共に、低酸素・低pH、栄養飢餓、炎症などの刺激とそれに対する応答により複雑な環境、いわゆる「がん微小環境」が構築されています。最近の研究では、がん微小環境ががんの増殖・浸潤・転移の促進に重要な役割を果たしていることが分かってきました。特にがん微小環境中の低酸素領域における炎症状態に着目し、それが「がんの悪性化進展にどのような影響を及ぼすのか?」、そしてそこには「どのような分子機序がはたらいているのか?」を明らかにするための研究を進めています。これにより、進行がんを対象とした新規の診断法や治療法の開発を目指します。

M. Akimoto
現在、「インターロイキン-33を標的とした炎症性がん微小環境の改善による治療戦略の検討」というテーマで研究を行っています。
※似顔絵は似顔絵イラストメーカーを使用して作成しました。

